Por qué esta página
Nuestra página web es una plataforma que ofrece una visión general acerca de las funciones de las barreras cerebrales así como cada uno de nuestros proyectos de investigación. Es una página dinámica, en constante desarrollo. Si tienes alguna pregunta, o te gustaría saber más sobre ciertos temas, ¡no dudes en contactarnos!
Nuestro objetivo es avanzar en el conocimiento científico de las barreras del cerebro y así acercarnos un poco más a la posibilidad de ayudar a los pacientes que sufren enfermedades cerebrales. Hemos desarrollado esta página web, BrainBarriers4You, para presentar las barreras del cerebro e informar acerca de los distintos proyectos de investigación dentro de la red BtRAIN.
Introducción
barrera cerebral
Introducción a la barrera cerebral
Nuestro cerebro es un órgano vital que necesita protección especial. Para ello, ciertas barreras lo defienden, como las murallas de un castillo. Estas barreras lo protegen de sustancias peligrosas, como las murallas del castillo impiden entrar a los enemigos, pero al mismo tiempo permiten la entrada de nutrientes y la salida de residuos. Por tanto, estas barreras son muy selectivas, pero cuando no funcionan bien, el cerebro empieza a desarrollar enfermedades. Por otra parte, puede ser que el cerebro enferme y necesite tratamiento. El problema es que las barreras que protegen el cerebro pueden impedir también que los medicamentos pasen, por lo que el cerebro no recibe el tratamiento adecuado. Es como si, por desgracia, los guardias en las murallas del castillo no pudiesen distinguir a los aliados de los enemigos, no dejando pasar a nadie. Este es el motivo por el que enfermedades como el Alzhéimer, la esclerosis múltiple y el cáncer cerebral son tan difíciles de tratar, y por tanto, necesitamos urgentemente una mejor comprensión de cómo funcionan las barreras cerebrales. Sólo entonces seremos capaces de diseñar medicamentos y estrategias para tratar esas enfermedades.
Contacto
Visite la página web oficial del proyecto BtRAIN para ponerse en contacto con los ESR o los miembros de la red.
¿Por qué tenemos barreras cerebrales?
Nuestro cuerpo está formado por órganos como el hígado, los riñones, los pulmones, los músculos y el cerebro, el cual, como una máquina bien engrasada, trabaja para permitirnos respirar, correr, pensar, reír y soñar, cada día y cada noche. El control de estas actividades reside en nuestro cerebro y espina dorsal, a los que conjuntamente llamamos el sistema nervioso central. Este sistema coordina la información que recibe del cuerpo y el ambiente que nos rodea, devolviendo señales a los músculos para movernos, a los pulmones para respirar, a los ojos para ver y a la boca para comer y hablar.
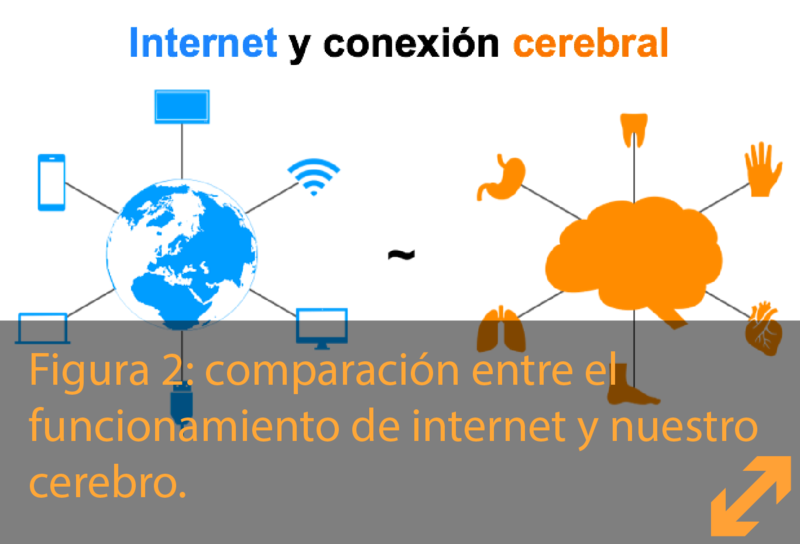
Este intercambio de información se realiza mediante unas células llamadas neuronas que, como en una red de internet, forman cables conectando nuestros órganos y músculos a diferentes centros de organización en el cerebro y, de vuelta desde este, se expanden para controlar el cuerpo.
El ambiente en el que están las neuronas debe mantenerse constante para que funcionen correctamente. La importancia de esto se comprueba en la intoxicación etílica. El alcohol es una molécula pequeña y especial que puede cruzar fácilmente las barreras cerebrales.
Cuando el alcohol entra en el cerebro altera la disponibilidad de nutrientes y la estabilidad de las neuronas, causando los conocidos trastornos de la embriaguez. ¡Imagina que todo lo que comiésemos o bebiésemos pudiera entrar fácilmente desde la sangre al cerebro! Nuestro cerebro necesita estar aislado de estas sustancias que pueden alterar la actividad cerebral. Además, nuestro cerebro también necesita protegerse de la invasión de organismos peligrosos como bacterias, hongos o virus. Por lo tanto, las barreras cerebrales permiten la entrada controlada de nutrientes mientras que se bloquea la entrada de sustancias tóxicas u organismos que podrían dañar el cerebro.
¿Sabías qué...?
El alcohol es una de las moléculas especiales que pueden atravesar la barrera hematoencefálica. Esto es posible porque es soluble en grasa. Otra palabra para grasa es lípido. Nuestras membranas celulares están formadas por una capa doble de estos lípidos parecida a una pompa de jabón, y por eso se caracterizan como ‘lipofílicos’, que significa afinidad por los lípidos.
La mayoría de las moléculas en la sangre son sólo solubles en agua y no pueden atravesar la membrana celular lipofílica. Estas moléculas se llaman "lipofóbicas", o que "temen a los lípidos". Sin embargo, las moléculas lipofílicas, como el alcohol, pueden entrar en el cerebro. Otro ejemplo son los analgésicos opioides como el tramadol. Afortunadamente, tramadol es lipofílico y por tanto puede entrar fácilmente en el sistema nervioso central para reducir nuestra percepción del dolor. Haloperidol, un antipsicótico típico, es otro ejemplo de medicamento lipofílico.
Lipofilia y lipofobia son por tanto características importantes a tener en cuenta al desarrollar medicamentos para tratar enfermedades cerebrales. Actualmente, aún no tenemos el conocimiento y las herramientas para abrir la barrera cerebral de forma segura y controlada. Por eso el tratamiento de enfermedades cerebrales se ve limitado al uso de moléculas lipofílicas.
⠀
Por eso necesitamos estructuras especializadas llamadas "barreras cerebrales" que separan el cerebro del resto del cuerpo y, como una muralla, lo protegen de la entrada de sustancias tóxicas y agentes infecciosos. Las barreras cerebrales no pueden ser completamente impenetrables, ya que en ese caso el cerebro no recibiría nutrientes. Por lo tanto, las barreras protegen de la entrada de material indeseado, y al mismo tiempo tienen transportadores para nutrientes y oxígeno de la sangre al cerebro. Es como una muralla con puertas vigiladas, que se pueden abrir para que los granjeros traigan los suministros.
¿Sabías que…?
Como en el resto del cuerpo, las células en el cerebro envejecen y mueren. Este proceso de muerte celular incluye a las neuronas. Durante un envejecimiento saludable, perdemos neuronas de forma natural, pero como tenemos suficientes neuronas para compensar, las funciones cerebrales no se ven perjudicadas. Sin embargo, una enfermedad puede afectar el cerebro destruyendo las neuronas, un proceso conocido como neurodegeneración. Esto ocurre en la enfermedad de Alzhéimer, en la que, por razones desconocidas, una molécula se acumula en el cerebro causando la muerte celular. Cuando se pierden demasiadas neuronas, el efecto en la función cerebral es evidente, como la pérdida de memoria en el Alzhéimer.
Barreras
en nuestro cerebro
La barrera hematoencefálica
La barrera hematoencefálica es una barrera que separa el cerebro de la sangre.
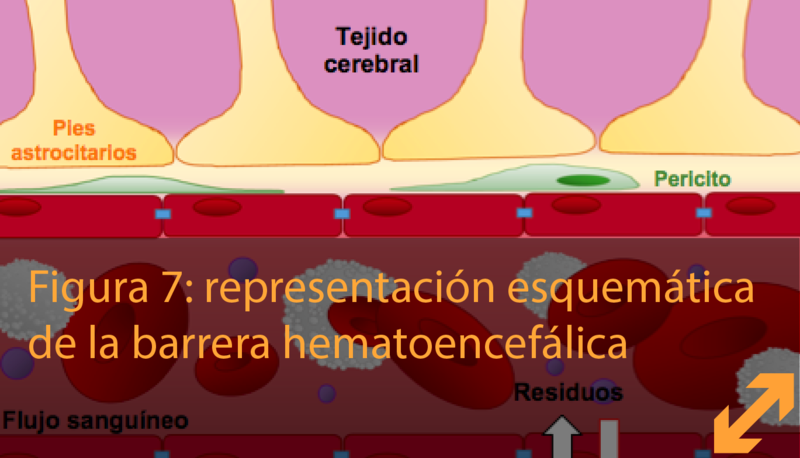
Nuestra sangre fluye por una red de vasos sanguíneos en cada órgano del cuerpo para transportar nutrientes esenciales y oxígeno, y de igual manera para eliminar residuos. El cerebro es un órgano muy dinámico y necesita un equilibrio delicado. Por otra parte, las sustancias dañinas que circulan en la sangre deben mantenerse fuera del cerebro. Estas sustancias pueden ser moléculas como toxinas, pero también patógenos como bacterias y virus. Esta regulación doble es posible gracias a la presencia de la barrera hematoencefálica, que está formada por un tipo especial de vasos sanguíneos: los capilares cerebrales. Estos capilares son los vasos sanguíneos más pequeños en el cerebro y consisten en miles de células colocadas una al lado de la otra formando tubos. Además, otros tipos de células participan en conferir a la barrera hematoencefálica sus propiedades de barrera.
¿Sabías qué…?
Los capilares del cerebro miden 650 km de largo y tienen una superficie de 20 m2.
1. Células endoteliales: la muralla de la barrera hematoencefálica
Las células endoteliales están conectadas formando el tubo de los vasos sanguíneos del cuerpo. Estas células tienen características diferentes dependiendo del órgano en el que estén. Por ejemplo, el hígado recibe sangre del corazón y la limpia además de absorber y distribuir los nutrientes de la digestión. Las uniones celulares entre las células endoteliales son muy laxas para poder absorber y procesar todo este contenido desde la sangre. Por otro lado, en el cerebro, las uniones entre las células endoteliales están muy fuertemente unidas.
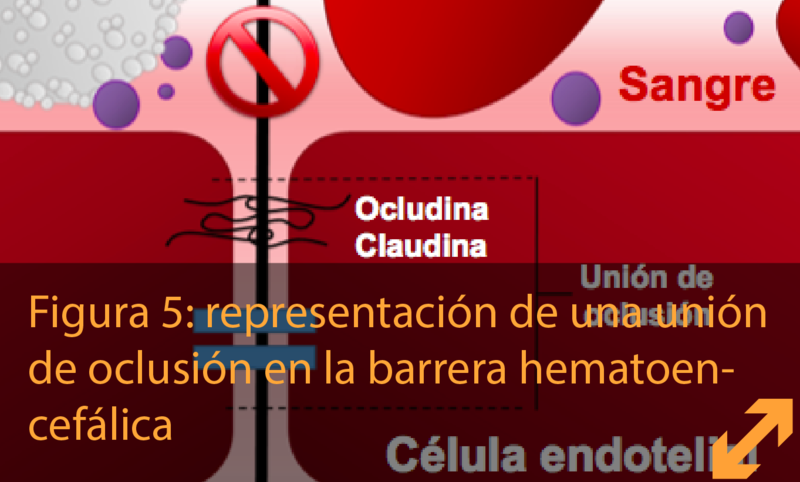
Las uniones entre las células endoteliales están formadas por moléculas especiales llamadas proteínas de adhesión celular. Estas proteínas actúan como una cremallera entre las células, permitiéndoles controlar la entrada de sustancias mediante la apertura y cierre de la cremallera (figura 5).
¿Sabías qué…?
La información para formar la estructura tan compleja y única de las proteínas se aloja en nuestro ADN. Consecuentemente, necesitamos mucha información en él, tanta, que si alineáramos todo el ADN de nuestras células, ¡podría dar la vuelta a la Tierra casi 3 veces!
Hay varios tipos diferentes de uniones que mantienen unidas a las células endoteliales. Algunas de estas uniones también están presentes en las células endoteliales que están fuera del cerebro. Estas uniones, llamadas “uniones adherentes”, pegan a las células entre sí impidiendo que, por ejemplo , los glóbulos rojos salgan de los vasos sanguíneos. Otro tipo importante de uniones presente en células endoteliales es particularmente fuerte en la barrera hematoencefálica. Cuando se observan a una magnificación muy elevada en el microscopio electrónico, las células aparecen firmemente unidas, por eso, a estas uniones se les llama uniones oclusivas o de oclusión. Las uniones de oclusión también se encuentran en otros tipos celulares de otros tejidos como hígado y riñón, y limitan el paso libre de moléculas y sales entre las células. Consecuentemente, estas conexiones actúan como una verdadera barrera física, similar a las paredes de una fortaleza. Las células endoteliales transportan nutrientes esenciales a través de esta barrera mediante el uso de transportadores especiales que actúan como camiones de transporte. La célula endotelial es similar a una empresa logística con camiones yendo y viniendo desde la sangre hasta la célula, y desde la célula hasta el cerebro. Además, cuando es necesario, la célula puede quedarse la carga específica de esos camiones para su uso propio (como el hierro, azúcares y sales). Por lo tanto, la unión de oclusión es una carretera sin paso, como una frontera cerrada y el paso a través de la célula está estrictamente controlado por la compañía logística.
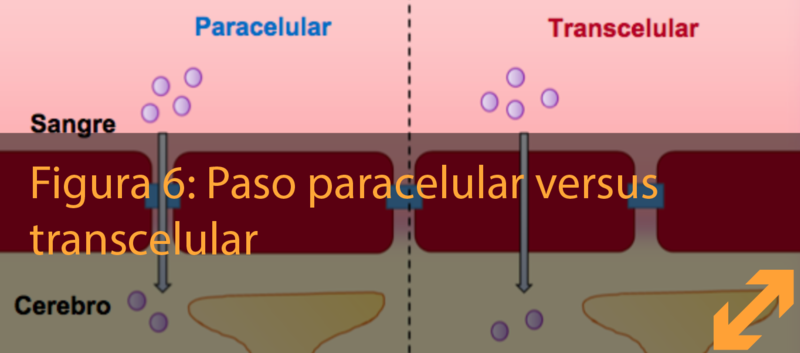
Para alcanzar el cerebro, las moléculas y células tienen diferentes maneras de atravesar la barrera hematoencefálica: "por entre las paredes de las células endoteliales" y "a través de la pared", conocidas como pasos paracelular y transcelular. Esta es una distinción importante a la hora de estudiar las filtraciones y los movimientos de moléculas y células a través de la barrera hematoencefálica.
¿Sabías qué...?
El ejercicio físico mejora nuestra memoria y función cognitiva. Estudios científicos han demostrado que la actividad física abre transitoriamente la barrera hematoencefálica. Algunos científicos debaten si esto permitiría el paso de factores que estimularían el crecimiento de las neuronas de nuestro centro de memoria, ayudando a hacer más inteligente nuestro cerebro.
2. Pericitos: un recubrimiento esencial
La palabra pericito deriva de "peri", que significa alrededor, y "cito", otra palabra para célula. Los pericitos son células contráctiles que cubren parcialmente los capilares envolviéndose alrededor de las células endoteliales como una hiedra. De esta manera, los pericitos cumplen con su papel importante de dar forma y estabilizar a los vasos sanguíneos. En el cerebro, estas células son importantes para mantener las características de barrera hematoencefálica de las células endoteliales.
La manera en la que los pericitos se conectan con las células endoteliales es mediante una envoltura fina entre y alrededor de ambas células llamada membrana basal, que ayuda a pegar las células entre si. Esta relación tan cercana permite a los pericitos regular el flujo sanguíneo bien contrayendo los vasos al disminuir su diámetro (vasoconstricción) –comparable a agarrar firmemente una manguera con nuestra mano– o soltando el agarre y aumentar su diámetro (vasodilatación). Esta interacción también otorga a los pericitos la posibilidad de comunicarse con las células endoteliales para regular filtraciones (también llamada permeabilidad).
Cuando los pericitos no funcionan adecuadamente, los residuos se acumulan, originando o empeorando patologías como la enfermedad de Alzhéimer.
3. Astrocitos: un apoyo importante
Los astrocitos son un tipo especial de células llamadas "células gliales" del cerebro, que dan apoyo y protección a las neuronas.
El cerebro consiste en dos tipos de células principales: neuronas y glía. El término "glía" literalmente significa "pegamento" o "relleno" y fue acuñado a este grupo de células porque inicialmente se creía que su función era simplemente mantener junto el cerebro. Las células gliales dan apoyo a las neuronas y ayudan a mantener el ambiente cerebral.
Las células gliales se pueden dividir en astrocitos, microglía (las células inmunes del cerebro) y oligodendrocitos (forman la capa de mielina aislante alrededor de los nervios).
Glial cells can be subdivided in astrocytes, microglia (the immune cells of the brain) and oligodendrocytes (forming the insulating myelin sheath around the nerves).
Los astrocitos son numerosos y diversos en el cerebro. Su nombre significa "células estrella" debido a su forma estrellada con muchas ramificaciones que les permiten alcanzar a las neuronas y los vasos sanguíneos.
Las ramificaciones que se prolongan hacia los vasos sanguíneos terminan de una forma específica parecida un pie pisando la superficie del vaso, y por eso se le denomina pie astrocitario . Estos pies permiten a los astrocitos actuar como mediadores entre las neuronas y la sangre. Gracias a estas conexiones, los astrocitos pueden, por ejemplo, regular la vasodilatación y vasoconstricción (de manera similar a los pericitos) de los vasos sanguíneos, disminuyendo o incrementando así el flujo sanguíneo. Además, los astrocitos mantienen la estructura de la barrera hematoencefálica al regular las interacciones entre las células endoteliales y los pericitos y estimular la formación de las uniones de oclusión endoteliales.
Explicación de 2 minutos sobre la barrera hematoencefálica: ![]()
¿Sabías qué?
En enfermedades como el Alzheimer o la epilepsia, donde se pierden muchas neuronas, los astrocitos tratan de reparar el tejido incrementando en número y cambiando su forma. Este proceso es muy parecido a la cicatrización pero no puede reemplazar la función de las neuronas.
La barrera sangre-líquido cefalorraquídeo
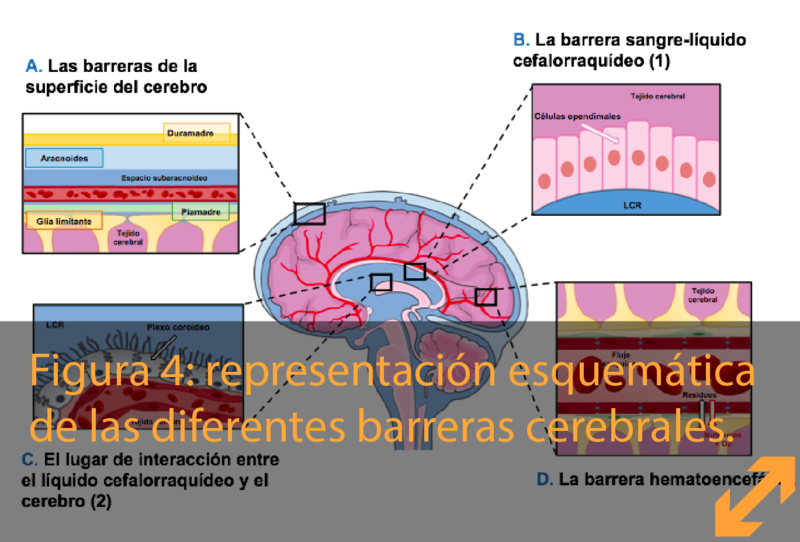
Nuestro cerebro está bien protegido de golpes no solo por el cráneo sino que también por un fluido especial que lo rodea y fluye a través de espacios por su centro, actuando de cojín. Este fluido , el líquido cefalorraquídeo (LCR), está producido por cuatro estructuras especiales distribuídas por el cerebro. A estas estructuras se las denomina "los plexos coroideos" (Figura 4). Éstos producen el LCR filtrando agua y nutrientes desde la sangre hasta el espacio en el que flota el cerebro.
Los vasos sanguíneos de los plexos coroideos no forman una barrera hermética sino que se conectan de forma laxa. En analogía a una fortaleza, estos vasos sanguíneos tienen las puertas constantemente abiertas sin que nadie controle el paso de mercancías a través de ellas. Sin embargo, hay una capa extra de células especializadas que cubren firmemente todo el plexo coroideo , las llamadas células epiteliales. Esta capa de células está en contacto con el LCR por un lado y la sangre por el otro, de manera que bombea líquido y nutrientes de la sangre al LCR.
Como el LCR baña todo el cerebro, es muy importante que la capa de células epiteliales de los plexos coroideos se mantenga hermética y regule apropiadamente lo que cruza, de manera similar a las células endoteliales de la barrera hematoencefálica. La barrera en los plexos coroideos es la denominada barrera sangre-LCR. Ésta actúa de portera manteniendo fuera las sustancias peligrosas y permitiendo la entrada de los nutrientes necesarios al LCR.
¿Sabías qué?
El cerebro humano contiene 150 mL de LCR. Dado que se renueva constantemente, el cerebro necesita fabricar medio litro cada día, del cual la mayoría se produce en los plexos coroideos.
¿Sabías qué?
Una función vital de la barrera sangre-LCR es la protección frente a infecciones. Lo consigue gracias al control del paso de células especializadas de la sangre denominadas células inmunitarias que, como policías, patrullan y comprueban nuestras células para combatir infecciones y células que actúen de forma disfuncional (como por ejemplo, células cancerosas). La importancia de esta vigilancia se manifiesta en las infecciones del cerebro: desafortunadamente, algunos virus y bacterias están especialmente equipados para atacar al cerebro y entrar por la vía de los plexos coroideos. Cuando las células inmunitarias que patrullan no consiguen matar a estos denominados patógenos, éstos pueden infectar el cerebro causando meningitis.
El estrecho control de la entrada de células inmunitarias es clave para un cerebro sano. En pacientes con esclerosis múltiple (EM), algunas células inmunitarias reconocen erróneamente células buenas como células malas, y piden refuerzos lanzando moléculas que activan al sistema inmune. Esto desemboca en una reacción en cadena que facilita este fenómeno de "auto"-ataque ("auto" significa "a uno mismo", y por eso la esclerosis múltiple se clasifica como una enfermedad auto-inmune) y recluta a más células en el cerebro. Esto sería efectivo al luchar contra infecciones, no obstante, al final estas células inmunitarias atacan al tejido cerebral en lugar de a la infección, produciendo el daño cerebral que causa los síntomas de la enfermedad.
El lugar de interacción entre el LCR y el cerebro
El interior de nuestro cerebro contiene cuatro espacios, llamados ventrículos, que están llenos de LCR. En el lugar de interacción entre en LCR y el cerebro hay una barrera creada por una sola capa de células epiteliales altamente especializadas, también conocidas como células ependimales. Esta capa de células ependimales no forma una barrera compacta como las barreras explicadas previamente, sino que está llena de huecos que la hacen muy permeable. Esto permite que el LCR difunda de dentro a fuera del cerebro. Esto contrasta con la capa de células epiteliales de los plexos coroideos donde el LCR se produce, ya que ésta está en contacto con los vasos sanguíneos y forma una auténtica barrera hermética entre la sangre y el LCR. La permeabilidad del lugar de interacción entre el LCR y el cerebro es muy importante para que la composición del LCR esté perfectamente regulada.
¿Sabías qué?
La barrera entre el LCR y el cerebro es probablemente una de las barreras menos estudiadas en el cerebro. Aun así, sabemos que posee funciones muy importantes que contribuyen al mantenimiento de una actividad normal del cerebro. Por ejemplo, las células ependimales tienen unas estructuras particulares llamadas cilios, como si fueran pelos diminutos (como las pestañas pero a escala celular), que se mueven en la misma dirección influenciando la dirección del LCR y a la vez filtrando sustancias peligrosas. Las células ependimales no están estrechamente conectadas entre ellas por lo que el LCR puede pasar al cerebro, permitiendo que los nutrientes y otros tipos importantes de sustancias alcancen a las neuronas.
Estudios recientes han demostrado que tras un derrame cerebral, las células ependimales pueden actuar de células sustitutas, esperando a que se les llame en caso de necesidad. De hecho, en el caso del derrame cerebral, estas células pueden entrar al cerebro y transformarse en neuronas, intentando así disminuir el daño cerebral causado por el derrame.
Las barreras de la superficie del cerebro
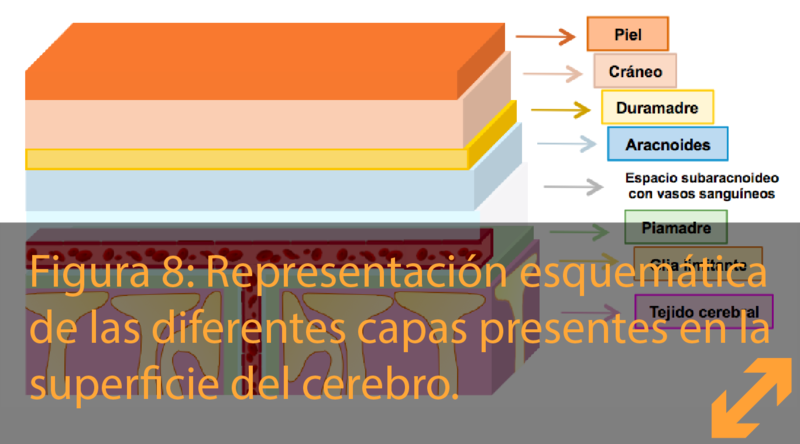
Yendo desde el cuero cabelludo hacia el cerebro, la primera protección contra los traumas es la estructura ósea del cráneo. Por debajo del cráneo y antes de alcanzar el cerebro, es necesario atravesar las meninges, tres capas que cubren y protegen al cerebro:
- La duramadre (o dura mater en latín), es la capa más externa, recubierta por el cráneo y la piel. Esta estructura es dura, protegiendo y sosteniendo al cerebro en caso de que el cráneo se fracturase en un accidente.
- La aracnoides (en griego "parecido a una araña o telaraña"), es la capa intermedia y la primera barrera real antes de alcanzar el cerebro.
- La piamadre (en latín "madre suave o tierna"), es la capa más interna de las meninges antes de alcanzar las primeras células del cerebro.
Hay un espacio entre la aracnoides y la piamadre llamado el espacio subaracnoideo. Este espacio está lleno de LCR, actuando como un cojín que absorbe los golpes en casos de movimientos bruscos de cabeza o traumas.
Para proteger de la entrada de elementos peligrosos a través de las meninges, las células de la aracnoides están firmemente conectadas mediante uniones de oclusión y aíslan el cerebro de forma similar a la barrera hematoencefálica. Por debajo de la piamadre existe una capa de astrocitos denominada glía limitante. No hay uniones de oclusión entre las células de la glía limitante. Esta capa controla el tráfico de células y moléculas entre el cerebro y la piamadre. Conjuntamente, las capas de las meninges completan el aislamiento del cerebro del resto del cuerpo, protegiéndolo.
¿Sabías qué?
La madre del cerebro
Los antiguos médicos árabes denominaron a las meninges alumm al-dimagh, que significa la madre del cerebro. Este término se tradujo más adelante al latín como mater.
Las barreras cerebrales: un campo dinámico todavía por descubrir
Aunque el estudio de las barreras cerebrales comenzó hace ya un siglo, los descubrimientos de hoy en día indican que el conocimiento actual sólo alcanza la punta del iceberg. Los avances tecnológicos en biología permiten la investigación de las características, la dinámica y los componentes celulares de la barrera hematoencefálica con una resolución creciente. Los esfuerzos combinados y colaboraciones entre científicos y el intercambio de datos internacional en las últimas décadas han sido esenciales para los avances en este campo. Dos temas prometedores que ahora somos capaces de abordar son la estructura dinámica de las barreras y las interacciones complejas entre las células que las forman.
Las barreras cerebrales: una estructura altamente dinámica
Aunque en condiciones saludables las barreras cerebrales están constantemente manteniendo un sistema nervioso central estable, esto no quiere decir que su status quo sea estático. En lugar de esto, las barreras son altamente dinámicas y se mantienen activamente durante toda la vida, adaptándose a situaciones diferentes.
Esto se pone en evidencia cuando, bajo ciertas condiciones a las que todos estamos expuestos, nuestras barreras cerebrales se pueden volver algo permeables. Por ejemplo, cuando tenemos una fiebre alta, en el mal de altitud o al hacer deporte extremo. Esto explica parcialmente por qué experimentamos un pequeño dolor de cabeza o confusión en esas circunstancias. Esta permeabilidad enfatiza lo dinámicas que son las barreras. Presumiblemente, es necesario que éstas sean a veces más rigurosas y en otros momentos más permeables, por razones que aún quedan por dilucidar.
La unidad neurovascular: formación de barreras mediante cooperación
Todas las células de la unidad neurovascular (células endoteliales, pericitos y astrocitos) interactúan y se comunican para regular las propiedades de las barreras.
Descubrimientos recientes apuntan a que los pericitos son esenciales para el transporte transcelular a través de la barrera hematoencefálica. Los pericitos dan instrucciones a las células endoteliales para que adquieran las características específicas de transporte, como si los pericitos fuesen el jefe ejecutivo de la empresa logística controlando los camiones que van y vienen a través de las células endoteliales. Hay diversos estudios en curso para que podamos entender la manera en la que los pericitos se comportan y poder así modular varias enfermedades.
Además, los astrocitos regulan la integridad de las uniones de oclusión entre las células endoteliales. Aunque la importancia de los astrocitos en modular estas uniones ya se conoce desde 1987, no fue hasta el 2011 en que los científicos fueron capaces de identificar la molécula exacta que los astrocitos envían a las células endoteliales para indicar que formen esas uniones.
Curiosamente, los pericitos también ayudan a los astrocitos a encontrar y rodear a los vasos con sus pies astrocitarios. La estrecha interdependencia de estas células demuestra el papel tan crítico que la comunicación juega entre todas las células para formar una barrera hematoencefálica correcta.
¿Qué es BtRAIN?
BtRAIN proyectos
¿Qué es BtRAIN?
BtRAIN proviene de la combinación de dos palabras en inglés: "brain" (cerebro) y "train" (entrenamiento o formación). Nuestro objetivo es la investigación de todos los aspectos relacionados con las barreras cerebrales; desde su formación temprana, funcionamiento y manipulación, hasta la investigación de enfermedades como la de Alzhéimer, esclerosis múltiple y el envejecimiento.
Los trastornos cerebrales afectan a mil millones de personas en todo el mundo, con cerca de 300 millones sufriendo de enfermedades como cáncer cerebral, esclerosis múltiple, Alzhéimer y Parkinson. A medida que nuestra sociedad envejece progresivamente, se espera que el número de enfermedades cerebrales aumente. Las terapias actuales proporcionan principalmente un alivio de los síntomas pero no detienen la progresión de la enfermedad, destacando la necesidad urgente de comprender mejor cómo funciona el cerebro y desarrollar nuevas estrategias y tratamientos.
BtRAIN se creó para reunir a investigadores de las barreras cerebrales de diferentes laboratorios repartidos por Europa y colaborar en un esfuerzo conjunto para analizar las funciones de las barreras cerebrales y desarrollar nuevas intervenciones terapéuticas. BtRAIN es una red europea de formación (ETN) de las acciones Marie Sklodowska-Curie (MSCA). Ésta proporciona programas de becas de investigación que apoyan a los estudiantes de doctorado (doctorandos) al combinar la investigación académica con la formación en industrias asociadas. Los doctorandos tienen la oportunidad de ganar experiencia en diferentes sectores y desarrollar cualificaciones transferibles al trabajar en proyectos de investigación conjunta. La red incluye 12 socios académicos y no académicos, cada uno de los cuales acoge a un doctorando y varios colaboradores de programas de capacitación. BtRAIN consta de 12 proyectos diferentes, uno ejecutado por cada doctorando, que se interconectan mediante colaboraciones. Los enlaces a los proyectos individuales se pueden encontrar aquí: http://www.btrain-2020.eu/esrOverview
Nosotros, los doctorandos de BtRAIN
Los proyectos de BtRAIN
ESR 1 – Marjolein Heymans
Modelos in vitro de la barrera hematoencefálica y aplicaciones en exámenes farmacológicos y toxicológicos.
En mi proyecto individual, pruebo diversos fármacos para el sistema nervioso central in vitro, que es un término que significa "en un tubo de ensayo" y es lo contrario a in vivo, que significa "en un organismo vivo". En mis experimentos uso diferentes tipos de células humanas y animales, con características de la barrera hematoencefálica, y las junto de manera que simulan una barrera hematoencefálica. Este tipo de experimentos reduce el uso intensivo y directo de los animales, permitiéndonos aún así estudiar los mecanismos de la barrera hematoencefálica. . El principal objetivo de mi proyecto es poder usar estos modelos in vitro para predecir la distribución de medicamentos en el cerebro humano, así como su toxicidad.
ESR 2 – Ana Raquel
Modelos in vitro de las barreras hematoencefálica y sangre-líquido cefalorraquídeo usando un dispositivo microfluídico integrado
Los vasos sanguíneos son parte del sistema circulatorio que transporta sangre por todo el cuerpo humano. Dos funciones importantes de los vasos sanguíneos son la separación y la conexión de la sangre y los órganos. La barrera hematoencefálica es una barrera selectiva que separa la sangre circulante del cerebro y el sistema nervioso. Debido a la complejidad de nuestro cerebro, el tratamiento de ciertas enfermedades (como el Alzhéimer, Parkinson, cáncer, etc) puede llegar a ser un verdadero desafío. Una forma barata y fácil de experimentar con la barrera hematoencefálica puede ser un modelo. Como un modelo de avión en un túnel de viento, las células de la barrera hematoencefálica se pueden cultivar en un canal fluídico bien diseñado. En este modelo podemos proporcionar las condiciones fisiológicas y controlar los parámetros cruciales de las células.
¿Qué podemos hacer, pues? Podemos imitar algunos trastornos del sistema. Modulamos los vasos sanguíneos del cerebro para encontrar tratamientos mejores. Es muy importante obtener nuevas herramientas para mejorar los estudios en tiempo real.
ESR 3 – Raoul F.V. Germano
Comparación de los transcriptomas de células endoteliales cerebrales de ratón y pez cebra e investigación funcional de vías conservadas que rigen la angiogénesis cerebral y la formación de la barrera hematoencefálica
A pesar del papel vital de la barrera cerebral endotelial para el funcionamiento adecuado del cerebro, sigue faltando un conocimiento detallado sobre cómo se constituye la formación de estos vasos sanguíneos. Para desentrañar genes nuevos implicados en la generación de la barrera endotelial, aprovechamos el pez cebra. Este modelo animal brinda la oportunidad de, usando embriones vivos, visualizar y manipular el desarrollo de los vasos sanguíneos y sus propiedades de barrera. Con el fin de encontrar los genes que son esenciales para la formación de las barreras cerebrales, examinamos los genes activos en el endotelio de la barrera hematoencefálica que están presentes tanto en el pez cebra como en la vasculatura del cerebro del ratón. La idea es que a medida que los vertebrados cambiaron a lo largo de la evolución de peces a mamíferos (mamíferos, incluidos humanos y ratones), los genes fundamentales para la formación de la barrera hematoencefálica se habrían mantenido en el proceso de selección natural. Por lo tanto, la comparación de ambas especies nos permite identificar esos genes "principales" que regulan la adquisición de propiedades de barrera por parte de las células endoteliales y luego seleccionar genes candidatos para estudiarlos con más detalle. Comprender la función de estos genes candidatos mejoraría nuestra comprensión de las enfermedades que afectan al cerebro y brindaría oportunidades para desarrollar estrategias alternativas para tratar a los pacientes que padecen estas enfermedades.
ESR 4 – David M. F. Francisco
Metanálisis integrativo de datos "ómicos" de la barrera hematoencefálica públicos y novedosos de vertebrados y establecimiento de la plataforma "BBBHub"
La información es importante. Sin embargo, para que la información sea útil, debe ser comprensible y accesible. El objetivo principal de mi proyecto es encontrar formas de ampliar la información que tenemos sobre la expresión génica (transcriptoma) en las barreras cerebrales. Para esto, colaboro con otros miembros de la red, analizando los datos de expresión que producirán. También estableceré metodologías para comparar los resultados y la calidad de los datos existentes. El resultado final será una plataforma web en la que se recopilará y analizará toda la información sobre la expresión génica de las barreras cerebrales, lo que permitirá a los científicos analizar, comparar y tener un mejor acceso a esta base de datos.
ESR 5 – Kakogiannos Nikolaos
El papel de la señalización del receptor acoplado a proteína G, Gpr126, en el desarrollo de la barrera hematoencefálica
La complejidad de la barrera hematoencefálica ha obstaculizado los esfuerzos para administrar fármacos al cerebro para el tratamiento de diversas afecciones patológicas, como cánceres y enfermedades neurodegenerativas. Con este propósito, debemos comprender la dinámica y los mecanismos moleculares que conducen a la formación de la barrera hematoencefálica a través de la identificación de genes nuevos. En nuestro laboratorio nos hemos centrado en un nuevo gen, Gpr126, que creemos que es importante para el desarrollo de la barrera hematoencefálica. Estamos tratando de describir el papel y el mecanismo molecular de Gpr126 durante el establecimiento de la barrera hematoencefálica.
ESR 6 – Eduardo Frías-Anaya
Doctorando 6 – Eduardo Frías-Anaya
Todos cambiamos al envejecer, es un proceso natural e imparable que afecta a nuestro cuerpo y sus múltiples funciones. Al igual que otros órganos, nuestro cerebro cambia a medida que envejecemos y sufre efectos variables que alteran nuestra cognición, memoria o nos hacen más susceptibles a enfermedades neurodegenerativas, pero también a incidentes vasculares (es decir, accidente cerebrovascular o derrame). Los incidentes neurovasculares están estrechamente relacionados con la barrera hematoencefálica, ya que durante el envejecimiento la función y la estructura de esta barrera se alteran y se vuelve permeable, lo que promueve el paso de compuestos del flujo sanguíneo al cerebro. Estos cambios a nivel de la barrera hematoencefálica parecen estar asociados con cambios en la expresión de varios genes y miARN (moléculas pequeñas que pueden estimular o bloquear la expresión de muchos genes). Estamos tratando de estudiar qué cambios de la expresión génica en la barrera hematoencefálica pueden relacionarse con las alteraciones estructurales y funcionales observadas en el envejecimiento.
ESR 7 – Ricardo M. Figueiredo
ARNs no codificantes derivados de la barrera hematoencefálica (BHE) como biomarcadores funcionales de la BHE envejecida versus la BHE en la enfermedad de Alzhéimer
Al ser la enfermedad de Alzhéimer una de las demencias más prevalentes en personas de edad avanzada y que afecta a casi 13,8 millones de personas en todo el mundo, es urgente encontrar un diagnóstico preciso, no invasivo y métodos de pronóstico. Actualmente, el diagnóstico preliminar del Alzhéimer se realiza mediante una combinación de criterios clínicos que incluye un examen neurológico, pruebas de estado mental e imágenes cerebrales. Sin embargo, con base en las pruebas clínicas anteriores, el diagnóstico del Alzhéimer se vuelve difícil, especialmente en pacientes que están en etapas leves o tempranas del Alzhéimer. Dado que las propiedades de la BHE están alteradas en los cerebros de los pacientes con Alzhéimer, esperamos que las células endoteliales expresen diferentes genes en esta afección. En consecuencia, diferentes moléculas pequeñas de ARN podrían liberarse en la sangre de pacientes con Alzhéimer. Por esa razón, desarrollaremos técnicas precisas para analizar la sangre y encontrar las moléculas de ARN provenientes de la BHE en mal estado. Si las moléculas de ARN encontradas en la sangre concuerdan con las que encontremos en las células endoteliales de la BHE en mal estado, podemos utilizar estas moléculas como biomarcadores funcionales para esta condición. Estas moléculas de ARN podrían usarse en el futuro para el diagnóstico del Alzhéimer.
ESR 8 – Luca Marchetti
Mecanismos endoteliales cerebrales que dirigen la vía celular de migración de células T a través de la barrera hematoencefálica (BHE)
La función de las células inmunitarias es protegernos de infecciones y agentes externos. Sin embargo, durante enfermedades autoinmunes, en condiciones que no se comprenden completamente, las células inmunes pueden volverse dañinas para nosotros mismos y atacar nuestro propio cuerpo. Durante la esclerosis múltiple, una enfermedad autoinmune del sistema nervioso central, las células inmunes pueden atravesar la BHE y causar daños en el cerebro. En mi proyecto tratamos de comprender las diferencias entre los mecanismos utilizados por dos tipos particulares de células inmunitarias para cruzar la BHE, que son las células T Th1 y Th17. Además, sabemos que las células T tienen dos vías posibles para cruzar la BHE: "entre las membranas celulares" y "a través de la membrana celular", conocidas como las vías paracelular y transcelular. En nuestro laboratorio, podemos estimular las células endoteliales de la BHE con condiciones que dirigen las células T preferentemente por trans o paracelular. Ambos enfoques nos ayudarán a tener una mejor comprensión de cómo las células T pueden cruzar la BHE durante la esclerosis múltiple.. Al identificar qué genes son cruciales en este proceso, nuestro objetivo es mejorar los tratamientos actuales para la esclerosis múltiple, intensificando la especificidad y reduciendo los efectos secundarios de los tratamientos.
ESR 9 – Amaia Dominguez-Belloso
Contribución de la barrera hematoencefálica en la biología del amiloide-β en la enfermedad de Alzhéimer
El amiloide-β es una de las dos moléculas principales que se acumulan en el cerebro de los pacientes con Alzhéimer, destruyendo las neuronas y causando los síntomas de pérdida de memoria que todos conocemos. BACE-1 es el nombre de la molécula que genera amiloide-β. Nuestro laboratorio mostró previamente que las células endoteliales de los vasos cerebrales contienen BACE-1 activado, lo que podría contribuir al Alzhéimer. Nuestro objetivo es comprender el papel de las células endoteliales en Alzhéimer, y esperamos descubrir nuevas dianas terapéuticas como BACE-1 en éstas células para tratar esta enfermedad tan terrible que afecta a una parte cada vez mayor de la población en los países occidentales.
ESR 10 – Markus Schuster
Exploración de las células T CD4+ como vehículos para mediar en el transporte de fármacos a través de la barrera hematoencefálica
Nuestro objetivo es desarrollar un sistema de transporte de fármacos que se pueda utilizar para facilitar el transporte de fármacos desde la sangre hasta el cerebro. Por lo tanto, los medicamentos se encapsulan en pequeñas nano-cápsulas llamadas polimerosomas, que se forman mediante el uso de polímeros biocompatibles y biodegradables. Para administrar esos polimerosomas a través de la barrera hematoencefálica al cerebro, los polimerosomas se unen a células T que tienen la capacidad innata de cruzar la barrera hematoencefálica y llegar naturalmente al cerebro . Después de que las células T hayan llevado los polimerosomas a su objetivo final, éstos se degradan con el tiempo hasta que se desprenden de las células y liberan su carga.
ESR 11 – Marie Wiatr
Papel de diferentes receptores en el fomento de la migración de patógenos y leucocitos a través de la barrera sangre-líquido cefalorraquídeo en la meningitis
Mi proyecto trata sobre cómo un virus puede cruzar la barrera sangre-líquido cefalorraquídeo e ingresar en el cerebro. Estoy trabajando en un virus específico que causa meningitis, el echovirus 30. Este virus altera la barrera y puede dañar el cerebro. Estoy intentando identificar cómo el virus puede ingresar en las células epiteliales de la barrera cerebral y por qué mecanismo y qué moléculas se adhieren para penetrar dentro de las células.
Cuando estás enfermo, células específicas, las células inmunes, están luchando contra los patógenos. Otra parte de mi trabajo es identificar cómo estas células inmunes entran en el cerebro cuando hay una infección.
ESR 12 – Sabela Rodríguez Lorenzo
Control molecular de las barreras cerebrales humanas en la salud y la neuroinflamación
Para mantener el ambiente delicado del cerebro, el líquido cefalorraquídeo que baña el cerebro se separa de la sangre por la barrera de sangre-líquido cefalorraquídeo en el plexo coroideo. Esta barrera es un guardián que evita la entrada de sustancias nocivas. En la esclerosis múltiple, las células del sistema inmune, que generalmente protegen al cuerpo de amenazas externas, pueden ingresar en el cerebro y atacar la vaina de mielina que rodea las neuronas.
Queremos entender qué falla en la barrera sangre-líquido cefalorraquídeo en la esclerosis múltiple. Utilizamos una técnica llamada "secuenciación de ARN" para comparar los perfiles de expresión génica en los plexos coroideos de pacientes con esclerosis múltiple y donantes sanos. El estudio de los genes alterados en los plexos coroideos de estas muestras humanas nos ayudará a comprender los mecanismos que contribuyen al funcionamiento de la barrera sangre-líquido cefalorraquídeo y esperamos que, en el futuro, puedan usarse como dianas farmacológicas para tratar la esclerosis múltiple.
Vídeos
relacionados con la barrera hematoencefálica