Warum diese Webseite
Unsere Website ist eine Platform, geschaffen um ihnen eine Möglichkeit zu geben, einen Einblick in die Funktion der Hirn-Schranken sowie in unsere Forschungsprojekte zu bekommen. Wir bieten ihnen eine dynamische Website, die ständig im Neuaufbau ist und aktualisiert wird. Sollten ihnen durch den Inhalt dieser Website neue Fragen aufkommen oder sollten sie weitere Informationen bezüglich eines speziellen Themas wollen, so sind sie herzlichst dazu eingeladen uns zu kontaktieren.
Unser Ziel ist es, das wissenschaftliche Verständnis der Hirn-Schranken zu verbessern und dabei einen Schritt näher daran zu sein, Patienten mit Hirnleiden zu helfen. Wir haben diese Website verfasst, um ihnen eine Einführung in die Thematik der Hirnschranken zu geben und sie über die Tragweite unserer Projekte im BtRAIN Konsortium zu geben.
Einleitung
Hirn-Schranken
Einführung in Gehirnschranken
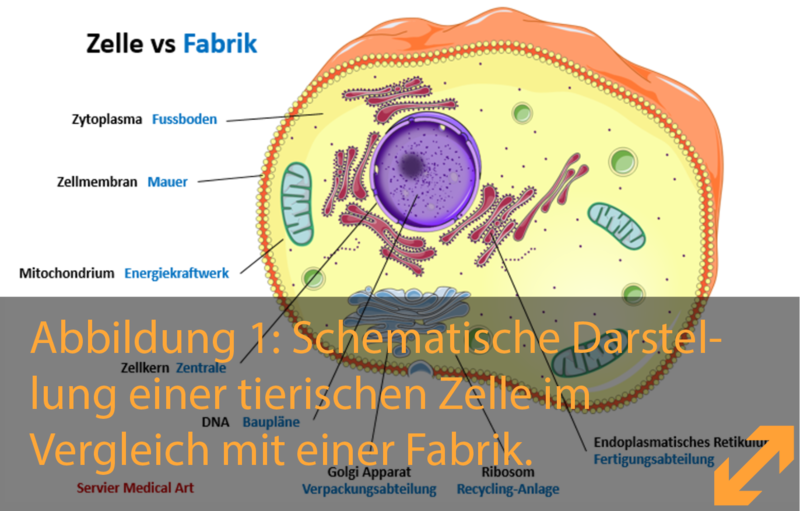
Da unser Gehirn ein sehr wichtiges Organ ist, muss es vom Körper geschützt werden. Deshalb gibt es Barrieren, die es schützen, wie die Mauern einer Festung. So wie Festungsmauern verhindern, dass ein Feind die Festung einnimmt, so verhindern diese Barrieren, dass gefährliche Stoffe in das Gehirn eindringen. Gleichzeitig erlauben sie aber den Transport von Nährstoffen in das Gehirn. Diese Schranken sind also äußerst selektiv. Wenn sie aber nicht mehr funktionieren, beginnt das Gehirn eine Krankheit zu entwickeln. So kann es passieren, dass das Gehirn erkrankt ist und an Behandlung bedarf. Das Problem ist aber, dass die gleichen Barrieren, die das Gehirn schützen, es auch vor Medikamenten abschottet, sodass das Gehirn nicht behandelt werden kann. Das wäre, wie wenn die Wächter einer Festung nicht Freund von Feind unterscheiden könnten und deshalb sicherheitshalber keinem von beidem den Zugang gewähren. Eben aus diesem Grund sind Krankheiten im Gehirn wie Alzheimer, MS und Hirntumore so schwer behandelbar. Und deshalb brauchen wir dringend ein besseres Verständnis für die Funktionsweise der Hirn-Schranken. Nur dann können wir in der Lage sein, Krankheiten im Gehirn zu heilen.
Contact
Bitte besuchen sie die offizielle Website für das BtRAIN Projekt, um die ESRs und die Netzwerkmitglieder zu kontaktieren. http://www.btrain-2020.eu/
Warum haben wir Hirn-Schranken?
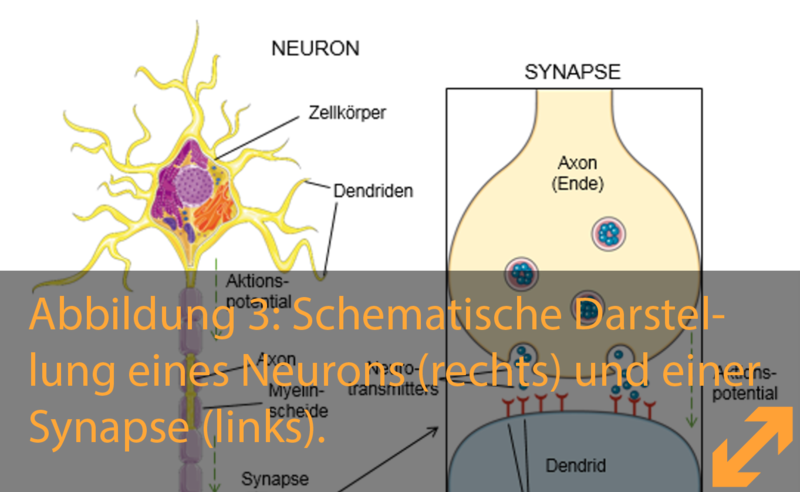
Unser Körper besteht aus einzelnen Organen, wie die Leber, die Nieren, das Herz, die Lunge, Muskeln und das Gehirn. All diese Organe müssen wie ein gut geöltes Uhrwerk eng zusammenarbeiten, damit wir Tag und Nacht atmen, rennen, denken, lachen und träumen können. Die zentrale Schaltstelle dazu besteht aus unserem Gehirn und unserem Rückenmark. Beides zusammen nennen wir das zentrale Nervensystem (ZNS). Das ZNS koordiniert alle Informationen, die es von unserem Körper über unsere Umgebung bekommt, verarbeitet sie und befiehlt anschließend unsere Muskeln, damit diese sich in Bewegung versetzen, unsere Lunge, damit diese atmen, unsere Augen, damit sich sie diese umschauen und unseren Mund, damit dieser isst und redet. Die Verarbeitung dieser Informationen übernehmen Zellen, die wir Neuronen nennen. Wie eine Internetverbindung, verbinden sie all unsere Organe und Muskeln zu einem Netzwerk mit verschiedenen Organisationszentren im Gehirn, und geben gleichzeitig unserem Gehirn eine Verbindung, um den Körper zu kontrollieren.
Für die Aktivität dieser Neuronen ist es von höchster Wichtigkeit, dass ihre Umgebung (unser Gehirn) konstant und ohne größere Schwankungen oder Störungen ist. Wie wichtig dies ist, kann am Beispiel einer Alkoholvergiftung gezeigt werden. Alkohol ist ein kleines Molekül, das trotz der Hirn-Schranken einfach in das Gehirn eindringen kann.
Wenn Alkohol ins Gehirn gelangt, verändert es die Verfügbarkeit von Nährstoffen und die Stabilität der Neuronen, was zu Trunkenheit führt. Stellen sie sich vor, das würde bei allem, das wir essen oder trinken passieren. Nach jeder Malzeit bräuchten wir ziemlich viel Zeit, um uns zu erholen! Die Aufnahme von Substanzen, die die Hirnaktivität verändern, muss also unterbunden werden. Desweiteren, muss das Gehirn vor gefährlichen Organismen, wie Krankheitserregern geschützt werden, da diese es sonst zerstören würden. Die Hirn-Schranken erlauben die kontrollierte Aufnahme von Nährstoffen, während sie gleichzeitig giftige Substanzen und Pathogene, die das Gehirn schädigen könnten, abblocken.
Haben sie schon gewusst?
Alkohol ist eines der wenigen Moleküle, dass die Blut-Hirn-Schranke überwinden kann, da es löslich in Fetten (auch Lipide genannt) ist. Unsere Zellmembranen bestehen aus einer Lipid-Doppelschicht und werden deshalb als lipophil (Fett liebend) eingestuft.
Die meisten Moleküle im Blutkreislauf sind nur in Wasser löslich und können die Lipid-Doppelschicht der Zellmembran nicht überwinden. Diese Moleküle sind lipophob (Fett meidend). Lipophile Moleküle wie Alkohol können über die Blut-Hirn-Schranke ins Gehirn gelangen. Ein weiteres Beispiel ist das Opioid Tramadol, ein Schmerzmittel. Tramadol ist lipophil und kann einfach ins ZNS gelangen, um dort unser Schmerzempfinden zu lindern. Ein weiteres Beispiel für ein lipophiles Medikament ist Haloperidol, ein Antipsychotikum.
Das Gleichgewicht zwischen Lipophilie und Lipophobie ist daher eine wichtige Eigenschaft, die berücksichtigt werden muss, wenn Medikamente entwickelt werden, die im Gehirn wirken sollen. Denn bis heute ist es noch nicht möglich, die Blut-Hirn-Schranke sicher und kontrolliert zu öffnen und zu schließen, weshalb Medikamente für Krankheiten im Gehirn auf lipophile Moleküle beschränkt sind.
⠀
Aus diesem Grund, brauchen wir hoch spezialisierte Strukturen, die Hirn-Schranken, die das Gehirn vom Rest des Körpers wie eine Festung abgrenzen und die Aufnahme giftiger und infektiöser Substanzen verhindern. Die Hirnschranken dürfen aber nicht komplett unüberwindbar sein, da das Gehirn sonst keine Nährstoffe erhalten und verhungern würde. Sie schützen das Gehirn vor dem Eindringen von Schadstoffen einerseits und andererseits besitzen sie hochspezifische aktive Transportmechanismen für den Transport von Nährstoffen und Sauerstoff aus dem Blut ins Gehirn, vergleichbar zu einer Festung mit bewachten Toren, die für Bauern geöffnet werden können, damit diese Vorräte in die Festung bringen können.
Haben sie schon gewusst?
Genau wie im Rest des Körpers, altern und sterben Neuronen in Gehirn. In einem gesunden Alterungsvorgang, verlieren wir auf natürliche Weise Neuronen, wobei die Hirnfunktionen uneingeschränkt bleiben, da wir genug restliche Neuronen besitzen, um die Abgestorbenen zu ersetzen. Auch bei neurodegenerativen Krankheiten sterben Neuronen ab, was das Gehirn diesmal aber beeinträchtigen kann. Genau dies passiert bei Alzheimer, bei der sich Schadstoffe ungewollt ansammeln und zum Tod von Neuronen führen. Wenn dann zu viele Neuronen abgestorben sind, wird der Effekt auf das Gehirn ersichtlich. Bei Alzheimer ist das der fortschreitende Gedächtnisverlust.
Schranken
in unserem Gehirn
Was sind die verschienden Hirn-Schranken?
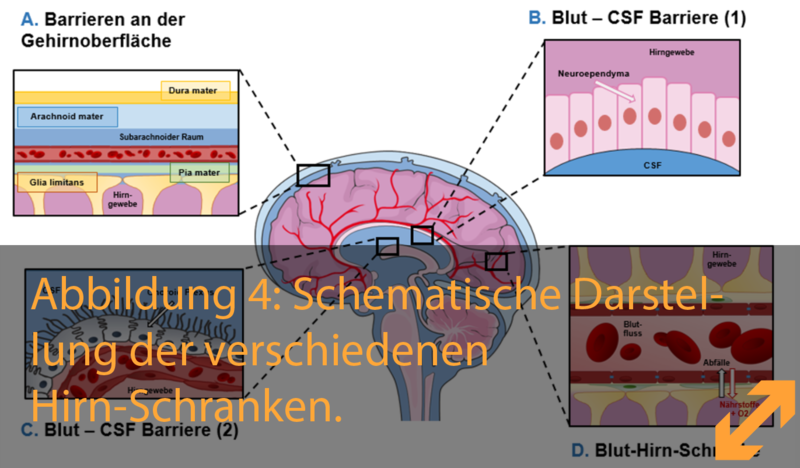
In unserem Körper gibt es verschiedene Arten von Hirn-Schranken (Abbildung 4):
Die Barrieren an der Hirnoberfläche
Die Blut-Zerebrospinalflüssigkeits-Barriere (BCSFB)
Die Blut-Hirn-Schranke (BBB, engl. von blood-brain barrier) und
die Grenzfläche zwischen der Zerebrospinalflüssigkeit und dem Gehirn.
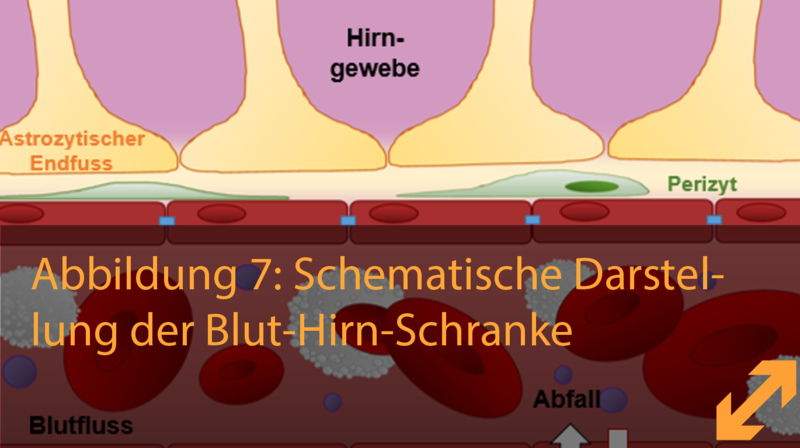
Die Blut-Hirn Schranke
Die Blut-Hirn-Schranke (blood-brain barrier, BBB) ist eine Barriere, die das Gehirn vom Blut abgrenzt.
Unser Blut fließt durch ein Netzwerk an Gefäßen in jedem Organ in unserem Körper, um diese mit essentiellen Nährstoffen und Sauerstoff zu versorgen und Abfallstoffe abzutransportieren. Das Gehirn ist ein sehr dynamisches Organ und es benötigt ein sehr fein eingestelltes Gleichgewicht. Es muss strengstens verhindert warden, dass Gifte und Pathogene, wie Viren und Bakterien, vom Blutkreislauf ins Gehirn gelangen und dort Schaden anrichten. Diese zwiespaltige Regulierung is wegen der Blut-Hirn-Schranke möglich, welche aus einer speziellen Art von Gefäßen besteht: Hirnkapilaren. Diese Kapilaren sind die kleinsten Blutgefäße in unserem Gehirn und bestehen aus tausenden zu Röhrchen aneinandergereihten Zellen. Zusätzlich zu diesen gibt es weitere Arten an Zellen, die daran beteiligt sind, der Blut-Hirn-Schranke ihre Eigenschaften zu verleihen. Diese stellen wir ihnen im Folgenden vor.
Haben sie schon gewusst?
Aneinandergereiht sind die Hirnkapilaren 650 km lang und haben eine Gesamtoberfläche von 20 m2.
1. Endothelzellen: Die Wand der Blut-Hirn-Schranke
Endothelzellen sind miteinander verbunden, um die Wand der Blutgefäße in unserem Körper zu formen. Diese Zellen haben je nach Organ verschiedene Eigenschaften. Zum Beispiel leitet die Leber das Blut vom Herz weiter. Sie nimmt das Blut auf, reinigt es und verteilt die Nährstoffe, die wir durch unsere Verdauung aufnehmen. Darum sind dort die Verbindungsstellen (engl. junctions) zwischen den Endothelzellen sehr durchlässig wie ein weitmaschiges Netz, sodass der komplette Blutinhalt aufgenommen und verarbeitet werden kann. Im Gegensatz dazu sind die Verbindungsstellen im Gehirn äußerst undurchlässig und eng miteinander verbunden.
Endothezellen sind miteinander durch spezielle Moleküle verbunden, die wir zelluläre Adhäsionsproteine (engl. cellular adhesion proteins) nennen. Diese Proteine wirken wie ein Reißverschluss zwischen den Zellen. Durch das Öffnen und schließen dieser Reißverschlüsse wird die Aufnahme von Substanzen aus dem Blut kontrolliert. (Abbildung 5)
Haben sie schon gewusst?
Die Bauanleitungen für diese komplexen und einzigartigen Proteine sind in unserer DNS gespeichert. Es befindet sich also ein riesiger Haufen an Informationen in unserer DNS. Würde man die DNS unserer Zellen aneinander reihen, so würde man mit ihr unsere Erde fast 3 mal umwickeln können.
Es gibt verschiedene Arten von Verbindungen, die unsere Endothelzellen zusammen halten. Eine dieser Verbindungen gibts es auch an Endothelzellen auserhalb des Gehirns. Diese Verdindungen kleben oder halten die Endothelzellen zusammen, um unteranderem zu verhindern, dass rote Blutkörperchen aus den Blutgefäßen austreten. Sie werden adherens junctions (engl.: adhärente Verbindungsstellen) genannt. Eine weitere äußerst wichtige Art von Verbindungen sind besonders stark und sind unter dem Microskop betrachtet besonders dicht zusammengereiht. Deshalb nennt man sie tight junctions (engl.: Dichte Verbindung). Tight junctions gibt es auch in anderen Organen wie der Leber und den Nieren. Sie schränken den freien Austausch von Molekülen und Salzen zwischen Zellen ein. Diese Verbindungen funktionieren also wie eine richtige physikalische Barriere, ähnlich den Mauern einer Festung. Durch spezielle Transporter, die wie LKWs funktionieren, transportieren Endothelzellen Nährstoffe über diese Barriere hinweg. Man könnte die Endothelzellen als eine Art Speditionsunternehmen ansehen, die mithilfe von LKWs Nährstoffe vom Blut zur Zelle transportiert und anschließend von der Zelle zum Gehirn und weiter. Die Endothelzellen können auch einen Teil der Fracht für sich behalten, wenn sie es benötigen (z.B. Eisen, Zucker und Salze). Die tight junctions sind also eine Art Grenze mit Grenzkontrolle und der Druchgang durch die Zellen wird strikt durch das Speditionsunternehmen kontrolliert.
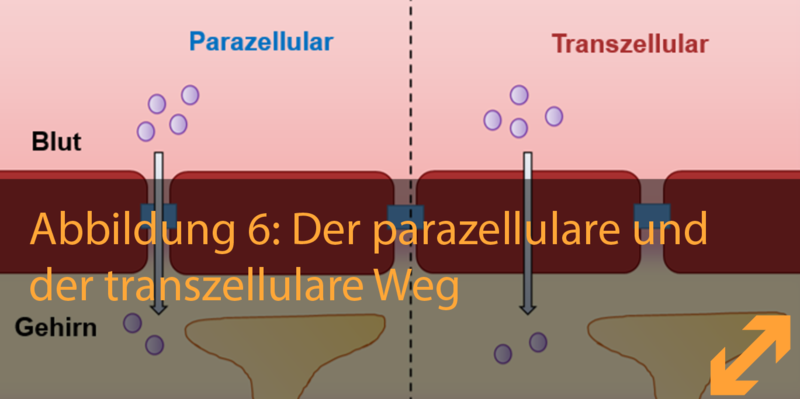
Um das Gehirn zu erreichen, stehen den Molekülen verschiedene Wege über die Blut-Hirn-Schranke zur Verfügung: Zwischen den Zellwänden zweier Zellen hindurch (parazellular) und durch die Wand einer einzelnen Zelle hindurch (transzellular). Diese Unterscheidung ist wichtig, wenn man die Undichtheit und die Bewegung von Molekülen oder Zellen über die Blut-Hirn-Schranke untersuchen will.
Did you know?
Physische Anstrengungen verbessern unser Gedächtnis und unsere kognitiven Funktionen. Studien haben gezeigt, dass sich die Blut-Hirn-Schranke bei physischen Anstrengungen vorübergehend leicht öffnet. Einigen Wissenschaftlern zufolge erlaubt dies das Eindringen von Stoffen in das Gehirn, die Neuronen stimulieren und es dem Zentrum für Gedächtnis im Gehirn erlaubt zu wachsen. Dies trage dazu bei, dass unser Gehirn schlauer wird.
2. Perizyten: Eine essentielle Ummantelung
Der Name Perizyt kann von den Wörtern „peri“, was „um etwas herum“ bedeuted und „zyt“, ein anderes Wort für Zelle, abgeleitet werden. Perizyten sind kontrahierbare Zellen, die die Blutkapillaren teilweise umhüllen, indem sie sich wie Efeu um die Endothelzellen ranken. Dadurch erfüllen sie ihre Funktion, das Formen und Stabilisieren der Blutgefäße. Im Gehirn, sind diese Zellen essentiell für den Erhalt der Barriereeigenschaften von Endothelzellen.
Perizyten und Endothelzellen sind durch eine spezielle dünne Schicht verbunden, die sich um und zwischen beiden Zelltypen befindet. Diese wird die basale Membran gennant und hilft die Zellen zusammen zu halten. Diese enge Beziehung ermöglicht es den Perizyten den Blutfluss zu regulieren, indem sie die Blutgefäße zusammenziehen (Vasokonstriktion) – vergleichbar zu einer Hand, die einen Schlauch zusammenquetscht, oder indem sie diesen Griff lockern (Vasodilation). Dieses Zusammenspiel ermöglicht es den Perizyten auch mit Endothelzellen zu kommunizieren und so die Dichtheit (auch Permeabilität) des Endothels zu steuern.
Wenn die Perizyten nicht richtig arbeiten, können sich Abfallprodukte anhäufen, was zu einer Verschlechterung der patologischen Zustände, wie zum Beispiel Alzheimer, führt.
3. Astrozyten: Eine wichtige Unterstützung
Astrozyten sind eine spezielle Art von Zellen im Gehirn, sogenannte Glialzellen, die die Neuronen unterstützen und schützen.
Das Gehirn besteht aus 2 Grundtypen von Zellen: Neuronen und Glia. Der Begriff Glia bedeutet buchstäblich „kleben“ oder „füllen“ und wurde diesen Zellen als Namen verliehen, da man dachte, Ihre Funktion sei es einfach das Gehirn zusammenzuhalten. Glialzellen unterstützen Neuronen und helfen das Milieu des Gehirns aufrecht zu erhalten. Glialzellen können in mehrere Gruppen unterteilt werden: die Astrozyten, das Mikrogla (die Immunzellen des Gehirns) und die Oligodendrozyten, die die isolierende Myelinschicht um die Nerven bildet.
Es gibt zahlreiche und unterschiedliche Astrozyten im Gehirn. Ihren Namen, „Stern-Zellen“, haben sie aufgrund ihrer Form mit vielen Auswucherungen bekommen. Diese erlaubt es ihnen sowohl die Neuronen als auch die Blutgefäße zu erreichen. Die Auswucherungen, die zu den Blutgefäßen führen, enden in einer speziellen Form, die aussieht als ob ein Fuß auf die Oberfläche des Blutgefäßes tritt. Deshalb werden diese End-Fuß genannt. Durch diese End-Füße können Astrozyten als Vermittler zwischen den Neuronen und dem Blut agieren. Zum Beispiel ermöglicht es diese Verbindung, die Vasodilation und Vasokonstriktion ähnlich wie bei Perizyten, wodurch der Blutfluss erhöht oder erniedrigt wird. Zusätzlich erhalten Astrozyten die Struktur der Blut-Hirn-Schranke, indem sie die Interaktion von Endothelzellen und Perizyten miteinander regulieren und die Bildung von thight junctions im Endothel fördern. Unter folgendem Link finden sie eine 2 minütige Einführung zur Blut-Hirn-Schranke: ![]()
Haben sie schon gewusst?
Bei Krankheiten wie Alzheimer oder Epilepsie, in denen zahlreiche Neuronen abgestorben sind, versuchen Astrozyten dieses Gewebe zu reparieren, indem sie sich vermehren und ihre Form ändern. Dieser Prozess ist erstaunlich ähnlich zum Prozess einer Narbenbildung, er kann aber die Funktion der Neuronen nicht ersetzen.
Die Blut-CSF-Barriere (BCFSB)
Unser Gehirn wird gegen Einschläge gut geschützt, nicht nur durch den Schädelknochen, sondern zusätzlich auch durch eine spezielle Flüssigkeit, die es umgibt und durchdringt und wie ein Airbag abfedern kann. Diese Flüssigkeit, die Zerebrospinalflüssigkeit (engl. cerebrospinal fluid, CSF), wird in vier speziellen Strukturen im Gehirn produziert, die wir „Choroid Plexus“ nennen (Abbildung 4). Sie produzieren die CSF indem sie Wasser und Nährstoffe aus dem Blut zum Gehirn hin filtern.
Blutgefäße im Choroid Plexus formen keine dichte Barriere, sondern sind lose miteinander verbunden. In Analogie zu einer Festung, hätten diese Blutgefäße dauerhaft offene Tore, ohne Wächter, die kontrolieren, wer oder was bei dem Tor ein- oder aus geht. Es gibt jedoch noch eine zusätzliche Schicht an Zellen, die den ganzen Choroid Plexus dicht umgeben, die Ephithelzellen. Diese Zellschicht grenzt an einer Seite an die CSF und an der anderen an das Blut und pumpt nährstoffhaltige Flüssigkeit vom Blut in die CSF.
Da das Gehirn in der CSF badet, ist es äußerst wichtig, dass die Epithelschicht des Choroid Plexus dicht bleibt und den Stoffaustausch strickt reguliert, vergleichbar zu Endothelzellen in der Blut-Hirn-Schranke. Die Barriere des Choroid Plexus nennen wir Blut-CSF-Barriere (BCSFB). Die BCSFB ist der Türsteher, der Schadstoffe draußen hält und den Eintritt von wichtigen Nährstoffen in die CSF erlaubt.
Haben sie schon gewusst?
Das menschliche Gehirn ist von 150mL CSF umgeben. Da diese ständig erneuert wird, muss das Gehirn jeden Tag einen halben Liter an CSF produzieren. Das meiste davon wird im Choroid Plexus produziert.
Haben sie schon gewusst?
Eine Hauptfunktion der BCSFB ist das Gehirn vor Infektionen zu schützen, indem es den Eintritt von Immunzellen aus dem Blut in die CSF kontrolliert. Immunzellen patroulieren und überprüfen unsere Zellen, um Infektionen und abnormale Zellen, wie Krebszellen, zu bekämpfen. Die Wichtigkeit dieser Überwachung wird bei Infektionen im Gehirn sichtbar: Leider sind einige Viren und Bakterien speziell dazu ausgestattet das Gehirn über den Choroid Plexus anzugreifen. Wenn diese Überwachung der Immunzellen fehlerhaft ist und die Pathogene nicht abtötet, dann können diese Pathogene das Gehirn infizieren, was zu einer Meningitis führt.
Eine strikte Kontrolle für den Eintritt von Immunzellen ist ein weiterer Schlüsselfaktor für ein gesundes Gehirn. Bei Patienten mit Multipler Sklerose (MS), werden gute Zellen fälschlicher Weise von den Immunzellen als schlechte Zellen erkannt, woraufhin die Immunzellen Verstärkung anfordern, indem sie Stoffe aussenden, die das Immunsystem aktivieren. Diese Lösen dann eine Kettenreaktion aus, die dieses „friedly fire“ Phänomen verstärkt und zu einer Autoimmunkrankheit führt, sodass immer mehr Immunzellen rekrutiert werden. Zwar würde dies effektiv sein, wenn es um den Kampf gegen Infektionen geht, jedoch greifen diese Immunzellen letztendlich Gehirngewebe an, was zu den Hirnschäden führt, die die typischen Symptome von MS auslösen.
Die Grenzfläche zwischen Blut und CSF
Unser Gehirn ist im Inneren in vier Bereiche, den Ventrikeln, aufgeteilt, die mit der CSF gefüllt sind. An der Grenzfläche zwischen CSF und dem Gehirn befindet sich eine Barriere, die aus einer einzelnen Schicht and hoch spezialisierten Epithelzellen, auch Ependymalzellen gennant, besteht. Diese Schicht aus Ependymalzellen formt keine abgeschlossene Barriere, wie die die vorher besprochen wurden, da sie löchrig und undicht ist. Dies erlaubt der CSF in das Gehirn und aus ihm heraus zu strömen, ganz im Gegensatz zu der Schicht an Epithelzellen am Choroid Plexus, wo die CSF produziert wird. Denn dort heften die Epithelzellen an den Blutgefäßen an, um eine richtige, dichte Barriere zwischen Blut und CSF zu bilden, der BCSFB. Da diese BCSFB so undicht ist, ist es umso wichtiger, dass die Zusammensetzung der CSF perfekt reguliert wird.
Haben sie schon gewusst?
Die Barriere zwischen CSF und Gehirn, ist die am wahrscheinlich schlechtesten untersuchte Barriere im Gehirn und dennoch wissen wir, dass die äußerst wichtige Funktionen erfüllt, die zu einer normalen Gehirnfunktion beitragen. Zum Beispiel haben Ependymalzellen bestimmte Hährchen-Strukturen, die Cilia genannt werden (wie Wimpern, aber im zellulären Maßstab). Indem die Cilia alle in die selbe Richtung schlagen, bestimmen sie so die Richtung der CSF und filtern Schadstoffe aus ihr heraus. Ependymalzellen sind nicht durch tight junctions miteinenader verbunden, was bedeutet, dass die CSF in das Gehirn gelangen kann und es so mit Nährstoffen und anderen wichtigen Substanzen versorgen kann. Aktuelle Studien haben ergeben, dass Ependymalzellen nach einem Schlaganfall als eine Art Ersatzspieler funktionieren können, um für den Fall der Fälle bereit zu stehen. Tatsächlich können Ependymalzellen nach einem Schlaganfall „auf das Spielfeld laufen“ und sich zu Neuronen umwandeln, um den Schaden des Schlaganfalls zu begrenzen.
Die Barrieren an der Gehirnoberfläche
Vom Schädelknochen zum Gehirn hin, ist die erste Schutzschicht die Knochenstruktur des Schädels. Darunter gibt es bis zum Gehirn drei weitere Schutzschichten:
- Die Dura Mater (Latein für “harte Mutter”): Sie ist die äußerste Schicht und ist mit Knochen und Haut überzogen. Diese äußerst resistente Schicht schützt das Gehirn und hällt im Falle eines Schädelbruchs alles zusammen.
- Die Arachnoid Mater (griechisch für “spinnennetzartige Mutter”): Sie ist die mittlere Schicht und die erste richtige Barriere vor dem Gehirn.
- Die Pia Mater (Latein für die “zarte Mutter”): Sie ist die unterste Schicht der Hirnhaut und befindet sich gerade vor den ersten Hirnzellen.
Den Raum zwischen Arachnoid Mater und Pia Matter nennt man subarachnoider Raum. Dieser Raum ist mit CSF gefüllt und wirkt wie ein Airbag, der Einschläge auf des Gehirn als Folge schneller Bewegungen oder Traumata abfedert.
Um den Eintritt von Schadstoffen durch die Hirnhaut zu verhindern, sind die Zellen der Arachnoid Mater durch tight junctions eng miteinander verbunden und grenzen das Gehirn wie bei der Blut-Hirn-Schranke ab. Unter der Pia Mater befindet sich eine Schicht an Astrozyten, die „Glia Limitans“ genannt wird. Zwischen den Zellen der Glia Limitans gibt es keine tight junctions. Die Glia Limitans kontrolliert die Zufuhr an Zellen und Molekülen von der Pia Mater zum Gehirn. All diese Schichten zusammen bilden die Grenze vom Gehirn zum Rest des Körpers und tragen somit zum Schutz des Gehirns bei.
Haben sie schon gewusst?
Die Mutter des Gehirns
Ärzte im frühen Arabien haben die Hirnhaut als alumm „al-dimagh“ bezeichnet, was soviel bedeutet wie „die Mutter des Gehirns“. Dieser Begriff wurde später wörtlich in das Lateinische als „mater“ übersetzt.
Hirn-Schranken: Ein dynamisches Thema, das noch erforscht werden muss
Obwohl die Forschung über die Hirn-Schranken über ein Jahrhundert zurück reicht, zeigen immer neue Entdeckungen, dass unser bisheriges Wissen nur die Spitze des Eisberges ausmacht. Der technische Fortschitt in der Biologie ermöglicht es, die Blut-Hirn-Schranke hinsichtlich Charakteristika, Dynamik und ihrer zellulären Bestandteile in immer detailierterer Auflösung zu untersuchen. Gemeinsame Anstrengungen und der Datenaustausch von Wissenschaftlern und internationalen Kollaborationen über die letzen Jahrzehnte waren essenziel für den Fortschritt in diesem Gebiet der Wissenschaft. Zwei bereits entstehende und sich entwickelnde Themen können wir mittlerweile angehen: Die Dynamik der Barrieren und die komplexen Interaktionen, in die die Zellen involviert sind.
Hirn-Schranken: Hoch flexible und dynamische Strukturen
Obwohl die Hirn-Schranken im gesunden Zustand durchgängig aktiv sind, um ein funktionsfähiges ZNS zu erhalten, bedeuted dies nicht, dass der „Status Quo“ der BBB statisch oder unflexibel ist. Stattdessen sind die Barrieren hoch dynamisch und werden während des ganzen Lebens aktiv gewartet, um sich den verschiedenen Situationen des Lebens anpassen zu können.
Sichtbar wird dies unter gewissen Umständen, unter denen die Hirn-Schranken leicht undicht werden. Zum Beispiel wenn wir Fieber haben, bei der Höhenkrankheit oder wenn wir Extremsport betreiben. Dies könnte erklären, warum wir unter diesen Umständen leichte Kopfschmerzen und Verwirrtheit verspüren. Die Undichtheit betont, wie dynamisch die Blut-Hirn-Schranke ist. Vermutlich müssen, aus Gründen, die wir nicht kennen, die Barrieren manchmal eher dicht und dafür zu anderen Zeiten etwas mehr undicht sein.
Die Neurovaskuläre Einheit: Formen einer Barriere zur Zusammenarbeit
Alle Zellen der neurovaskulären Einheit (Endothelzellen, Astrozyten und Perizyten) interagieren und kommunizieren miteinander, um die Barriere-Eigenschaften zu regulieren.
Jüngste Erkenntnisse betonen wie essentiel Perizyten für den transzellulären Transport über die Blut-Hirn-Schranke sind. Als ob sie der CEO eines Logistikunternehmens wären, der die Ein- und Ausfuhr aller LKWs, die die Endothelzellen passieren, kontrolliert, weisen die Perizyten die Endothelzellen an, spezifische Transportaufgaben zu erfüllen. Mehrere aktuelle Studien befassen sich damit, besser zu verstehen, wie sich Perizyten verhalten und den Verlauf verschiedener Krankheiten beeinflussen können.
Zur Ergänzung regulieren Astrozyten die Integrität der tight junctions zwischen den Endothelzellen. Wie wichtig Astrozyten bei dem Abdichten der Endothelzellen sind, wurde bereits 1987 entdeckt, aber erst 2011 konnten Wissenschaftler den genauen Signalstoff identifizieren, der von den Astrozyten abgesondert wird, um die Endothelzellen dazu zu bringen tight junctions auszubilden.
Interessanter Weise helfen Peryzenten den Astrozyten auch dabei Blutgefäße zu finden und mit ihren End-Füßen zu umgeben. Die engen Wechselwirkungen zwischen diesen Zellen zeigt, wie wichtig die Rolle der Kommunikation zwischen allen Zelltypen, die an der Aufrechterhaltung einer intakten Blut-Hirn-Schranke beteiligt sind, ist.
Was ist BtRAIN?
BtRAIN projects
What is BtRAIN?
Der Begriff BtRAIN setzt sich aus den englischen Wörtern "brain" (Gehirn) und "to train" (trainieren) zusammen. Unsere Aufgabe ist es, alle Aspekte der Hirn-Schranken zu untersuchen: von deren frühen Entstehung über deren Funktion und Manipulation bis hin zur Erforschung von Alzheimer, Multipler Sklerose (MS), Meningitis und der Alterung der Hirn-Schranken.
Über eine Milliarde Menschen sind weltweit von Krankheiten im Gehirn betroffen. Von diesen leiden etwa rund 300 Millionen Menschen an Krankheiten wie Gehirntumoren, MS, Schlaganfällen, Alzheimer und Parkinson. Da unsere Gesellschaft immer älter wird, wird erwartet, dass diese Zahlen immer weiter steigen. Moderne Therapien behandeln meistens nur die Symptome und stoppen nicht das Fortschreiten der Krankheit. Dies verdeutlicht, dass wir die Funktion des Gehirns besser verstehen müssen, um neue Methoden und Therapien für diese Krankheiten entwickeln zu können. Obwohl wir riesige Fortschritte für das Verständnis über die Entwicklung und Funktion der Hirn-Schranken gemacht haben, fehlt es uns noch immer an dem Wissen, das wir benötigen, um Therapien für Krankheiten, die auf der Fehlfuntion der Hirn-Schranken beruhen, zu entwickeln.
BtRAIN wurde gegründet, um Hirnforscher verschiedener Forschungsgruppen aus ganz Europa zusammenzubringen, um in gemeinsamer Zusammenarbeit die Funktion der Hirn-Schranken zu erforschen und neue Therapieansätze zu entwickeln. BtRAIN ist ein europäisches Trainingsnetzwerk (ETN) der Marie Sklodowska-Curie actions (MSCA). Letzteres, stellt Stipendien für Doktoranden (auch Early Stage Researchers oder ESRs genannt) zur Verfügung in denen es Forschung in der Wissenschaft mit Trainingsprogrammen in der Industrie verbindet. ESRs haben die Gelegenheit verschiedene Aspekte der Forschung zu erfahren und interdisziplinäre Fähigkeiten durch das Arbeiten in gemeinsamen Forschungsprojekten zu entwickeln. BtRAIN besteht aus 12 verschiedenen Projekten, die alle durch Kollaborationen miteinander verbunden sind. Eines für jeden ESR. Links zu den einzelnen Projekten finden sie auf folgender Webseite: http://www.btrain-2020.eu/esrOverview
Die BtRAIN Projekte
ESR 1 – Marjolein Heymans
In vitro Modelle der Blut-Hirn-Schranke und Anwendungen in pharmakologischen und toxikologischen Screenings
In meinem Projekt teste ich verschiedene Medikamente für das ZNS in vitro, was so viel bedeutet wie “im Reagenzglas”. Das Gegenteil wäre in vivo, also in einem lebenden Organismus. In meinen Experimenten mache ich von verschiedenen Arten von menschlichen und tierischen Zellen gebrauch, um sie in einer Weise zusammenzusetzen, dass sie die Charakteristika der Blut-Hirn-Schranke nachahmen. Diese Art an Experimenten vermindern den direkten und exzessiven Gebrauch von Tierversuchen, geben uns aber auch die Möglichkeit, die Barrierefunktionen der Blut-Hirn-Schranke zu erforschen. Das Hauptziel meines Projekts ist es, durch „in vitro“ – Modelle die Verteilung von Medikamenten im menschlichen Gehirn und deren Toxizität im Gehirn zu erforschen.
ESR 2 – Ana Raquel
In vitro-Modelle der Blut-Hirn-Schranke und der BCSFB basierend auf integrierten mikrofluidischen Systemen
Blutgefäße sind Teil eines Flüssigkeit-Kreislaufs, der Blut im gesammten Körper transportiert. Zwei wichtige Aufgaben dieser Gefäße sind die Trennung des Bluts von den Organen und der Stoffaustausch zwischen beiden. Die Blut-Hirn-Schranke ist eine selektive Barriere, die das zirkulierende Blut vom Gehirn und dem Nervensystem trennt. Da unser Gehirn zu komplex ist, wird es zu einer Herausforderung Krankheiten wie Alzheimer und Parkinson zu therapieren. Eine kostengünstige und einfache Methode, wäre es, ein Model für die Blut-Hirn-Schranke zu entwickeln. Wie ein Modelflugzeug in einem Windkanal, können Zellen der Blut-Hirn-Schranke in einem richtig designten Flüssigkeitskanal kultiviert werden. In einem solchen Modelansatz, können wir physiologische Bedingungen einbeziehen und die ausschlaggebenden Parameter der Zellen vermessen.
Was ist also machbar? Wir können einige Krankheiten in diesem System nachahmen. Wir verändern Gefäße im Gehirn, um bessere Therapien zu entwickeln. Um Echtzeitergebnisse von Studien zu verbessern, ist es von äußerster Wichtigkeit, neue Möglichkeiten zu erschließen.
ESR 3 – Raoul F.V. Germano
Der Vergleich der Transkriptome zerebraler Endothelzellen zwischen Maus und Zebrafisch und funktionelle Erforschung gemeinsam erhaltener Bildungsmechanismen für die Blut-Hirn-Schranke und Gefäße im Gehirn
Trotz der lebenswichtigen Rolle der endothelialen Hirn-Schranke für eine angemessene Gehirnfuntion, fehlt das Wissen über die Entwicklung dieser Blutgefäße. Um neue Gene zu erschließen, die an der Entwicklung dieser endothelen Barriere beteiligt sind, nutzen wir die Vorzüge eines Zebrafisch-Models. Dieses Tiermodel bietet uns die Möglichkeit in lebenden Embryonen die Entwicklung der Blutgefäße und deren Barriere-Eigenschaften zu beobachten und zu manipulieren. Um Gene zu finden, die essentiel für die Entwicklung der Hirn-Schranken sind, beobachten wir die Aktivität von Genen, die es sowohl im Endothel der Hirn-Gefäße von Zebrafischen als auch in denen von Mäusen aktiv sind. Die Idee ist, dass uns fundamentale Gene für die Entwicklung der Blut-Hirn-Schranke durch die natürliche Auslese hinweg erhalten geblieben sind, als wir Vertebraten uns durch die Evolutionsgeschichte hindurch von Fischen zu Säugetieren entwickelt haben. Indem wir beide Spezies vergleichen, können wir deshalb „Kerngene“ für die Entwicklung des Endothels und der Barriere-Funktionen identifizieren und Gene auszuwählen, die weiter erforscht werden sollen. Das Verständnis über diese Gene soll unser Verständnis über Krankheiten im Gehirn und deren Einfluss auf dieses verbessern und uns Möglichkeiten geben, alternative Strategien zur Behandlung von Patienten zu finden, die an diesen Krankheiten leiden.
ESR 4 – David M. F. Francisco
Integrative Meta-Analyse neuer und öffentlich zugänglicher Omics Daten über die Blut-Hirn-Schranke von Vertebraten und Erstellung des BBBHUBs
Informationen sind wichtig. Aber damit diese auch nützlich sind, müssen sie verständlich und verfügbar sein. Das Hauptziel meines Projektes ist es Möglichkeiten zu finden, die Informationen, die wir über das Transkriptom, also die Gesamtheit der Übersetzungsprodukte aller aktiven Gene, der Hirn-Schranken haben, zu erweitern. Dazu arbeite ich eng mit anderen Forschern unseres Netzwerks zusammen, um die Daten, die diese über die Expression der Gene erheben, zu analysieren. Desweiteren, führe ich Methoden ein, die es erlauben, existierende Daten hinsichtlich deren Ergebnisse und ihrer Qualität zu vergleichen. Das Endresultat wird eine Internetplattform sein, in der alle Informationen über die Expression der Gene der Hirn-Schranken gesammelt und analysiert werden. So wird Wissenschaflern in diesem Gebiet ein besserer Zugang dieser Daten-Sets ermöglicht, sodass diese die Daten-Sets einfacher analysieren und besser vergleichen können.
ESR 5 – Kakogiannos Nikolaos
Die Rolle des Signalwegs des G-Protein gekoppelten Rezeptors Gpr126 in der Entwicklung der Blut-Hirn-Schranke
Die Komplexität der Blut-Hirn-Schranke macht es schwer, Medikamente geziehlt im Gehirn zu verabreichen, um verschiedene pathologishe Zustände des Gehirns wie Krebs oder Neurodegeneration zu therapieren. Deshalb, ist es wichtig, dass wir die Dynamik und die molekularen Mechanismen, die die Entwicklung der Blut-Hirn-Schranke vorantreiben, verstehen, indem wir neue Gene dafür identifizieren. Unser Labor ist auf ein solches neuartiges Gen, und zwar das für Gpr126, spezialisiert, von dem wir glauben, dass es eine wichtige Rolle in der Entwicklung der Blut-Hirn-Schranke spielt. Deshalb erforschen wir die Rolle und die molekularen Mechanismen von Gpr126 während der Entwicklung der Blut-Hirn-Schranke.
ESR 6 – Eduardo Frías-Anaya
Die altersbedingte Veränderung in der Expression von Genen und mikroRNA in der Blut-Hirn-Schranke von Mäusen
Wir alle verändern uns während wir altern. Dies ist ein natürlicher und unverhinderbarer Prozess, der unseren Körper und seine Funktionen beeinflusst. Genau wie andere Organe, verändert sich unser Gehirn, wenn wir altern, und leidet under verschiedenen Effekten, die unsere Wahrnehmung und unsere Erinnerung beeinflussen oder uns mehr anfällig für neurodegenerative Krankheiten und neurovaskuläre Störungen, wie einem Schlaganfall, machen können. Neurovaskuläre Störungen sind direkt auf die Blut-Hirn-Schranke zurückzuführen. Beim Altern ändern sich die Funktion und die Struktur dieser Barriere und sie wird undicht, was den Übergang von Blutbestandteilen in das Gehirn erleichtert. Diese Änderungen auf Ebene der Blut-Hirn-Schranke scheinen mit der Änderung in der Expression verschiedener Gene und der miRNA (das sind kleine Moleküle, die die Expression von Genen beeinflussen können) verbunden zu sein. Wir versuchen zu erforschen, welche potentiellen Veränderung in der Expression von Genen in der Blut-Hirn-Schranke mit strukturellen und funktionellen Veränderungen, die beim Altern beobachtet werden können, einhergehen.
ESR 7 – Ricardo M. Figueiredo
Aus der Blut-Hirn-Schranke stammende, nicht kodierende RNAs als funktionelle Bio-Marker für eine alternde Blut-Hirn-Schranke im Vergleich mit der Blut-Hirn-Schranke in Alzheimer
Da Alzheimer eine der verbreitensten Formen von Demenz bei alten Menschen ist und fast 13.8 Millionen Menschen weltweit betrifft, ist es wichtig eine präzise und nicht-invasive Methode zur Diagnose von Alzheimer zu entwickeln. Heutzutage wird die Diagnose Alzheimer aufgrund einer Kombination von klinischen Kriterien getroffen. Dazu gehören eine neurologische Untersuchung, Tests über den Geisteszustand des Patienten und bildgebende Verfahren für das Gehirn. Speziell für Patienten mit leichtem Alzheimer oder Alzheimer im frühen Stadium ist es jedoch schwierig eine Diagnose für Alzheimer nur mit den obengenannten klinischen Test zu stellen. Da die Eigenschaften der Blut-Hirn-Schranke sich in den Gehirnen von Alzheimer Patienten verändern, erwarten wir, dass Endothelzellen bei diesen Patienten andere Gene exprimieren. Folglich sollten im Blut von Alzheimer Patienten andere der kleinen RNA Moleküle freigesetzt werden als bei gesunden Menschen. Aus diesem Grund, wollen wir hoch sensitive Methoden entwickeln, die es erlauben das Blut von Alzheimerpatienten auf diese kleinen RNA Moleküle zu untersuchen und deren Ursprung bei der Fehlfunktion der Blut-Hirn-Schranke zu finden. Falls die kleinen RNA Moleküle im Blut mit denen übereinstimmen, die bei einer Fehlregulation der Endothelzellen in der Blut-Hirn-Schranke gefunden werden können, dann können wir diese als funktionelle Bio-Marker für Alzheimer verwenden, sodass diese RNA Moleküle in Zukunft für die Diagnose von Alzheimer verwendet werden können.
ESR 8 – Luca Marchetti
Endotheliale Mechanismen im Gehirn, die den zellulären Weg der T-Zell Migration über die Blut-Hirn-Schranke bestimmen
Die Aufgabe von Immunzellen ist es, uns vor Infektionen und körperfremden Stoffen zu schützen. Jedoch können Immunzellen in Autoimmunerkrankungen durch Einflüsse, die wir noch nicht richtig verstehen, schädlich für uns werden und unseren eigenen Körper angreifen. Bei Multipler Sklerose, einer Autoimmunkrankheit unseres zentralen Nervensystems, können Immunzellen die Blut-Hirn-Schranke überwinden und unser Gehirn schädigen. Mein Projekt befasst sich mit den Unterschieden der Mechanismen, die zwei bestimmte Arten an Immunzellen, und zwar die Th1 und Th17 T-Zellen, verwenden um die Blut-Hirn-Schranke zu durchdringen. Desweiteren, wissen wir, dass es zwei Wege für die T-Zellen über die Blut-Hirn-Schranke gibt. Der eine führt zwischen den Zellwänden zweier Zellen hindurch (der parazellular Weg) und der andere durch die Zellwand einer einzelnen Zelle hindurch (der transzellulare Weg). In unserem Labor können wir die Endothelzellen der Blut-Hirn-Schranke so stimmulieren, dass die T-Zellen bevorzugt den parazellularen oder den transzellularen Weg einschlagen. Durch die Verwendung moderner Technologien (RNA Sequencing) haben wir eine Gesamtansicht aller aktiven Gene, die es ermöglichen, die T-Zellen in den einen oder den anderen Weg zu lenken. Beide Wege helfen es uns besser zu verstehen, wie T-Zellen die Blut-Hirn-Schranke in Patienten mit Multipler Sklerose überwinden können. Durch die Erforschung der Gene, die diesen Prozess beeinflussen, versuchen wir bestehende Therapien für MS zu verbessern, indem wir die Spezifität der Medikamente erhöhen und ihre Nebeneffekte vermindern.
ESR 9 – Amaia Dominguez-Belloso
Der Einfluss der Blut-Hirn-Schranke in der Biologie von Amyloid-β bei Alzheimer Patienten
Amyloid-β (Aβ) ist eines der beiden Moleküle, die sich hauptsäuchlich in den Gehirnen von Alzheimer Patienten ansammeln und so Neuronen abtöten, was zu dem Gedächtnisverlust führt, den wir alle kennen. BACE-1 ist das Molekül, das Aβ herstellt, und wir haben bereits in unserem Labor gezeigt, dass Endothelzellen von Blutgefäßen im Gehirn aktives BACE-1 enthalten, das potentiell zur Entstehung von Alzheimer beitragen könnte. Unser Ziel ist es die Rolle von Endothelzellen in Alzheimer zu verstehen und neue therapeutische Ziele in den Endothelzellen, sowie BACE-1, zu entdecken.
ESR 10 – Markus Schuster
Die Erforschung von CD4+ T-Zellen als Träger von Nanopartikeln, um den Transport von Medikamenten über die Blut-Hirn-Schranke zu erleichtern
Unser Ziel ist es, ein neuartiges Shuttle-System für Medikamente zu entwickeln, um deren Transport vom Blut zum Gehirn zu erleichtern. Dazu werden die Medikamente in kleine, aus gut verträglichen und biologisch abbaubaren Polymeren bestehende, Nano-Kapseln, genannt Polymersome, geladen. Um diese Polymersome über die Blut-Hirn-Schranke zu transportieren, heften wir diese an T-Zellen, die die Blut-Hirn-Schranke auf natürliche Weise überqueren, um in ihrem natürlichen Habitat, dem Parenchyma des Gehirns, zu verweilen. Nachdem die T-Zellen die Polymersome an ihr Ziel gebracht haben, werden die Partikel über die Zeit hinweg abgebaut, bis sie sich von den Zellen loslösen und ihren Inhalt freigeben.
ESR 11 – Marie Wiatr
Die Rolle verschiedener Rezeptoren bei der Förderung der Pathogen- und Leukozytenmigration über das BCSFB bei Meningitis
Mein Projekt dreht sich um die Frage, wie Viren die Blut-Hirn-Schranke überqueren und ins Gehirn gelangen können. Deshalb arbeite ich mit einem speziellen Virus (Echovirus 30), das Meningitis verursachen kann. Dieses Virus verursacht eine Störung der Blut-Hirn-Schranke und kann in Folge das Gehirn schädigen. Ich versuche herauszufinden, wie das Virus die Epithelzellen des Gehirns befallen kann und über welchen Mechanismus und welche Moleküle sich das Virus an die Epithelzellen anheften kann, um in sie einzudringen. Ein weiterer Bestandteil meiner Arbeit ist es, zu erforschen, wie diese Immunzellen im Falle einer Infektion in das Gehirn eindringen, um diese Krankheitserreger zu bekämpfen.
ESR 12 – Sabela Rodríguez Lorenzo
Molekulare Kontrolle der menschlichen Gehirnbarrieren in Gesundheit und Neuroinflammation
Um die leicht störbare Mileu im Gehirn zu erhalten, badet es in der Zerebrospinalflüssigkeit (CSF), die von dem Blut durch die Blut-Zerebrospinalflüssigkeits-Barriere (BCSFB) im Choroid Plexus getrennt wird. Diese Barriere verhindert den Eintritt von Schadstoffen in die CSF. Bei Patienten mit Multipler Sklerose, können Immunzellen, die normalerweise den Körper vor Pathogenen schützt, in das Gehirn eindringen und die Myelinscheiden, die die Neuronen umgeben, zerstören. Wir erforschen, was genau bei MS in der BCSFB gestört ist. Dazu nutzen wir eine Methode, die sich „RNA-Sequencing“ nennt, um die Expressionsprofile von Genen im Choroid Plexus von gesunden Menschen mit denen von MS Patienten zu vergleichen. Indem wir die Veränderungen in den Genen des Choroid Plexus dieser Menschen erforschen, können wir hoffentlich dazubeitragen, den Mechanismus, der zu einer intakten BCSFB-Funktion führt zu verstehen und diese Gene in Zukunft als therapeutische Ziele zur Behandlung von MS zu nutzen.
Videos
über Hirnschranken